
Сяалінь Бай, Цзін’янь Сян,
Цзяншань Дэн, Ван Хай Дын,
Сінхуа Луань і Чжы Гэн
Neurology. 2024 Mar 12; Volume 102 Number 5, e209188
У 30-гадовай жанчыны праз 1 месяц пасля перанясення COVID-19 паўстала хутка прагрэсавальная дэменцыя.
Паўторны аналіз спіннамазгавой вадкасці паказаў выяўленую гипогликорахию, у той час як пасевы, метагеномнае секвеніраванне і цитопатологическое тэставанне спіннамазгавой вадкасці давалі адмоўныя вынікі. Лабараторныя даследаванні, выкананыя ў рамках дыягнастычнага пошуку, выявілі падвышаны ўзровень аміяку ў крыві і CA-125. На МРТ галаўнога мозгу было выяўлена двухбаковае сіметрычнае дыфузнае кортикальное паражэнне. Дадзеныя змены на МРТ мелі лёгкую гіперінтэнсіўнасць на Т1-ўзважаным малюнку і назапашвалі кантраснае рэчыва. Больш дбайны збор анамнезу і спецыяльныя даследаванні пасля паказалі на этыялогію. Дадзены клінічны выпадак ілюструе падыход да дыягностыкі маладога пацыента з хутка прагрэсавальнай дэменцыяй, цяжкай гипогликорахией і дыфузнымі паразамі ЦНС, падкрэсліваючы важнасць шырокага дыягнастычнага пошуку.
Частка 1
У клініку паступіла 30-гадовая жанчына, у якой на працягу папярэдняга месяца назіраліся прагрэсавальнае зніжэнне памяці і афазія Брока. За 1 дзень да паступлення пацыентка магла выконваць бухгалтарскую працу самастойна. Якія адбыліся незадоўга да паступлення ў клініку атручвання і ўкусы насякомых, а таксама абцяжараны сямейны анамнез пацыентка адмаўляла. Адным месяцам раней у пацыенткі быў станоўчы ПЦР-тэст на SARS-CoV-2, тады ж пацыентка адчувала ліхаманку, кашаль і стомленасць. На момант паступлення ліхаманкі ў пацыенткі не было. Агульны агляд выявіў гіганцкія прыроджаныя меланоцитарные невусы (ВМН) на ніжніх канечнасцях (мал. 1А). З неўралагічнага пункту гледжання ў яе не было ніякіх дэфіцытаў, акрамя значнай кагнітыўнай дысфункцыі: па кароткай шкале ацэнкі псіхічнага статусу (Mini-mental State Examination, MMSE) пацыентка набрала 22 бала з 30. У пацыенткі назіраліся значныя , але пры гэтым захоўваліся здольнасці да разумення, арыентацыі і рахунку. На працягу 5 дзён стан пацыенткі рэзка пагоршылася: па MMSE пацыентка набірала ўжо 15 балаў з 30, а афазія стала змешанай. МРТ галаўнога мозгу паказала дыфузную гиперинтенсивность на Т1-ўзважаным малюнку (T1WI) (мал. 1B), падвышаную інтэнсіўнасць у рэжыме FLAIR (мал. 1C), назапашванне кантраснага рэчывы (мал. 1D) і адсутнасць абмежавання дыфузіі.
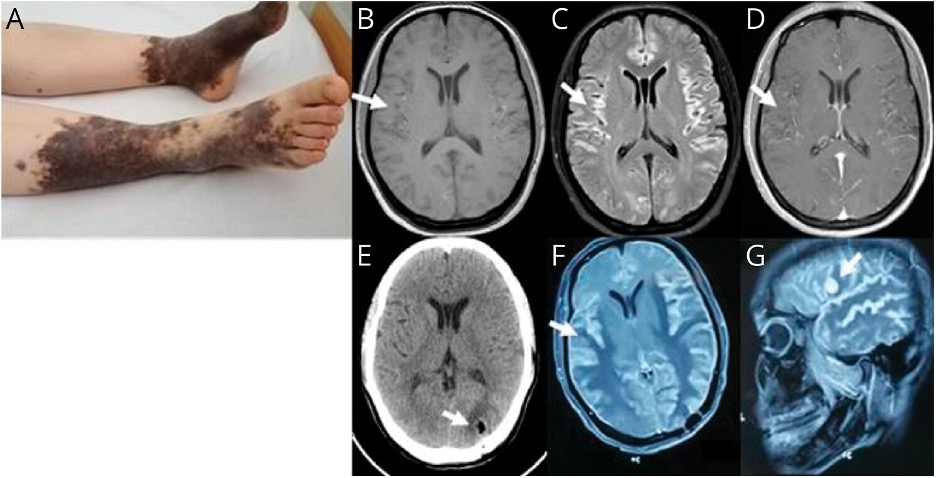
Малюнак 1
(А) Вялікія прыроджаныя меланоцитарные невусы (ВМН) няправільнай формы з множнымі сатэлітнымі невусамі на ніжніх канечнасцях, МРТ выявіла злёгку дыфузную гиперинтенсивность двухбаковых паўшар’яў галаўнога мозгу на T1WI (B), падвышаную інтэнсіўнасць | рэчывы (D). (Е) Пасляаперацыйная КТ на 2-ы дзень. Паўторная МРТ праз 6 месяцаў выявіла прадэманстравала больш тоўстыя і распаўсюджаныя пашкоджанні з ацёкам (F), а таксама з’яўленне новага агменю, які назапашвае гадаліній, у левай лобнай долі (G).
Пытанні да часткі 1
- Які дыферэнцыяльны дыягназ?
- Якія далейшыя крокі трэба зрабіць у абследаванні пацыенткі?
Частка 2
Дыферэнцыяльны дыягназ уключаў запаленчае / аутоіммунных захворванняў (што было вельмі верагодным, улічваючы COVID-19 ў анамнезе), інфекцыйнае захворванне (магчымасць віруснай або бактэрыяльнай каінфекцый выключаць было нельга), парушэнне метабалізму (напрыклад, гіпаглікемічных энцэфалапат першаснай меланомы скуры), нейродегенеративное захворванне (напрыклад, хвароба Крейтцфельдта-Якаба), судзінкавыя захворванні і атручванні (менш верагодныя, улічваючы хуткасць развіцця і адмаўленне пацыенткай шкодных уздзеянняў у анамнезе).
Тэставанне выявіла падвышаны ўзровень аміяку ў крыві (54 мкмоль / л, норма = 9-30 мкмоль / л) і CA-125 (56,81 Адз / мл, норма = 0-35 Адз / мл). Іншыя даследаванні, у тым ліку ацэнка функцыі печані, шчытападобнай залозы, нырак, запаленчых і імуналагічных паказчыкаў, аналізы на інфекцыі (гепатыт, пранцы, вірус імунадэфіцыту чалавека (ВІЧ) і туберкулёз), ўзроўні креатинфосфокиназы, лактатдегидроген МР-венаграфія галаўнога мозгу, прадэманстравалі нармальныя вынікі. Паўторны аналіз на аміяк, тандэмная мас-спектраметрыя крыві і мачы і КТ брушнай паражніны выключылі метабалічныя і анкалагічныя прычыны захворвання, што дазволіла выказаць здагадку, што павышаныя ўзроўні аміяку і CA-125 маглі на самой справе быць фізіялагічнымі. На 24-гадзінным ЭЭГ-маніторынгу адзначалася фонавая актыўнасць у бэта-дыяпазоне з частай тэта-дэльта-і спайкавай або спайк-павольна-хвалевай актыўнасцю ў абодвух паўшар’ях, без перыядычных разрадаў і эпилептических прыступаў. Першапачатковы аналіз спіннамазгавой вадкасці выявіў: пачатковы ціск 80 мм воднага слупа (норма = 80-180 мм воднага слупа); лейкацыты 9 × 10 ^ 6/л; эрытрацыты 348 × 10 ^ 6/л; бялок 0,63 г / л (норма = 0,15-0,45 г / л); глюкоза 0,29 ммоль / л (норма = 2,5-3,3 ммоль / л) пры ўзроўні глюкозы ў сыроватцы 3,9 ммоль / л. Паколькі кагнітыўныя парушэнні пагоршыліся, праз 5 дзён была праведзена другая люмбальная пункцыя, якая выявіла ўзровень глюкозы 0,28 ммоль / л пры ўзроўні глюкозы ў сыроватцы 7,2 ммоль / л. Паўторныя пасевы спіннамазгавой вадкасці (на вірусы, грыбы і мікабактэрыі), ПЦР-тэсты на вірус простага герпесу (ВПГ) і SARS-CoV-2, метагеномнае секвенаванне новага пакалення, а таксама сералагічныя скрынінг сыроваткі і паранеапластычная сіндромы далі адмоўныя вынікі.
Пытанні да часткі 2
- Які дыферэнцыяльны дыягназ гипогликорахии?
- Які дыферэнцыяльны дыягназ гіперінтэнсіўных змяненняў на T1-ВІ МРТ?
- Якія далейшыя крокі Вы зрабілі для пастаноўкі канчатковага дыягназу?
Частка 3
Гіпаглікорахія звычайна звязана з бактэрыяльным, вірусным (напрыклад, ВПГ, ВІЧ і COVID-19), грыбковым, сухотным і сіфілітычнае менінгітам. карцынаматозным менінгіце, субарахноідальном кровазліцці і гранулематозным ангііце ЦНС. На МРТ нашу ўвагу прыцягнулі гіперінтэнсіўныя нутрачарапныя ачагі на Т1-ВІ, якія маглі быць абумоўлены не такім і вялікім шэрагам прычын: такі сігнал маглі даваць. і меланін.Першымі варыянтамі дыягназу, з улікам гіганцкіх ВМН, гіперінтэнсіўнага сігналу на T1-ВІ МРТ і выяўленай гипогликорахии (суадносіны узроўняў глюкозы ў спіннамазгавой вадкасці і сыроватцы складалі <0,1), меланоз.Для пацверджання анкалагічнай этыялогіі былі праведзены даследаванні цыркулююць опухолевых клетак (ЦОК), цытапаталогія спіннамазгавой вадкасці і ПЭТ-КТ ўсяго цела з 18F-фтордезоксиглюкозой Два апошніх даследаванні далі адмоўны вынік, а аналіз на цок скуры патылічнай долі галаўнога мозгу (мал. 1E) не выявіла злаякасных наватвораў у скуры, але паказала чорную пігментацыю ў тканіны галаўнога мозгу (мал. 2А).
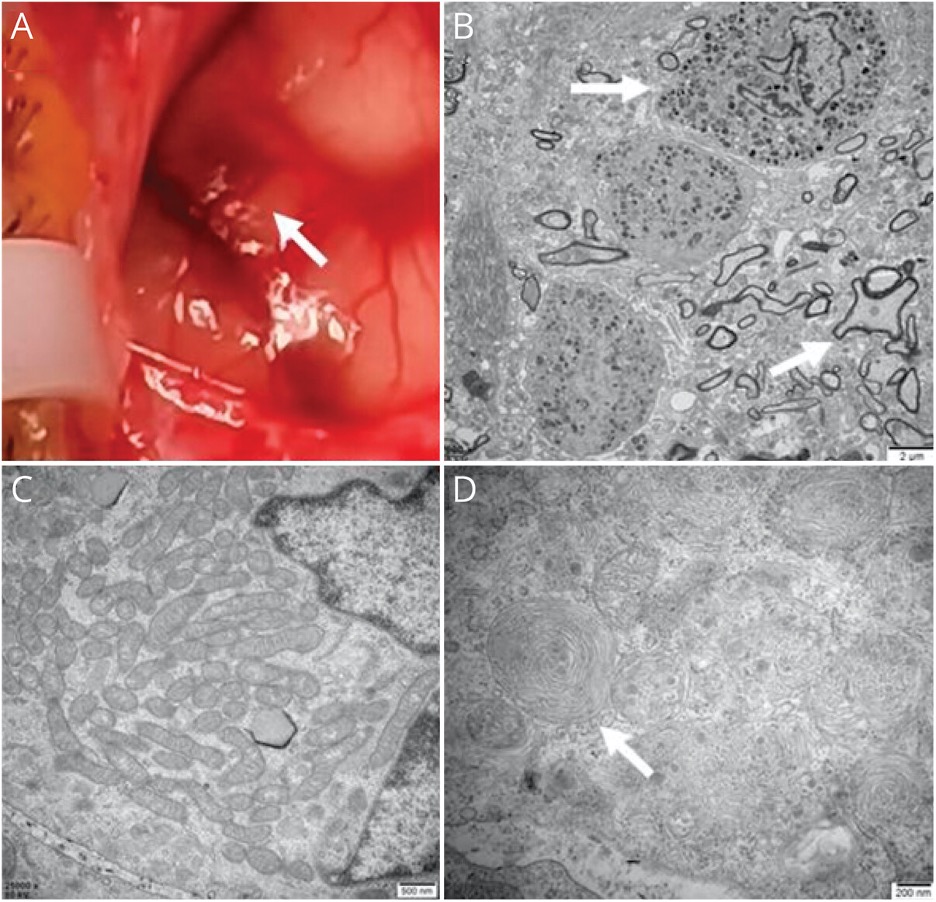
Малюнак 2
(А) Плямісты меланін (стрэлка) на мяккай і павуцінневай абалонках мозгу. (У) Назіралася вялікая колькасць меланоцитов ў тканіны галаўнога мозгу (стрэлка) і асанальная дэгенерацыя з дэміелінізацыяй нервовых валокнаў (стрэлка). (D) У нейроне былі выяўленыя аб’яднаныя ў кластары мітахондрыі і патэрны, якія нагадваюць адбіткі пальцаў (стрэлка).
Гистопатологическое даследаванне паказала круглявыя опухолевые клеткі, якія растуць па субпіяльнай прасторы і часткова інфільтруе парэнхіму галаўнога мозгу, раўнамерна размеркаваныя ў выглядзе гнёздаў з ўмеранай атыпіяй і адсутнасцю некрозу. Імунагістахімія паказала моцнае афарбоўванне на S100, SOX10, Melan A і HMB45, што казала пра меланоцитарной прыродзе пухліны. Малекулярны аналіз меланоцитомы выявіў мутацыю NRAS Q61K. Электронная мікраскапія паказала, што меланоциты знаходзіліся ў перываскулярнай прасторы з павелічэннем колькасці меланосам і мітахондрый (мал. 2, B і C). Акрамя таго, назіраліся аксональная дэгенерацыя, дэміэлінізацыя нервовых валокнаў і патэрны, якія нагадваюць адбіткі пальцаў (якія паказваюць на лізасамальную дысфункцыю, патэнцыйна звязаную з дэкампенсацыі кліранс меланіну) (мал. 2, B і D). На падставе клінічных дадзеных, МРТ, ПЭТ-КТ і біяпсіі пацыентцы быў пастаўлены дыягназ нейрокожный меланоз (НКМ).
На падставе клінічных дадзеных, МРТ, ПЭТ-КТ і біяпсіі жанчыне пастаўлены дыягназ «нейраскурны меланоз (НКМ)». Дыягнастычнымі крытэрыямі НКМ з’яўляюцца:
- буйныя (> 20 см у дарослых, 6-9 гл у дзяцей) або множныя (≥ 3) прыроджаныя меланоцитарные невусы (ВМН) з меланоз або меланомай ЦНС;
- адсутнасць меланомы скуры (за выключэннем пацыентаў без меланомы галаўнога мозгу);
- адсутнасць менінгеальнай меланомы (за выключэннем пацыентаў без злаякасных новаўтварэнняў скуры).
Мы таксама разглядалі магчымасць спадарожнай энцэфалапатыі, звязанай з COVID-19, хоць яна менш верагодная з-за часовай дынамікі сімптомаў. Першапачаткова пацыентка атрымлівала эмпірычную супрацьінфекцыйную і супрацьэпілептычную тэрапію. З-за высокай таксічнасці, нізкай адчувальнасці пухліны і няздольнасці выказваць пакуты хіміятэрапія і прамянёвая тэрапія не ўжываліся. Пасля стараннага абдумвання магчымых опцый лячэння для барацьбы з магчымай энцэфалапатыяй, асацыяванай з COVID-19, пацыентцы былі прызначаны пульс-тэрапія метилпреднизолоном (нутравенна, 1 г/дзень, на працягу 5 дзён / 0 г/г/г// на працягу 5 дзён). На жаль, паляпшэння стану пацыенткі не назіралася. Яе стан пагоршылася на працягу 6 месяцаў; за гэты час у пацыенткі развіліся генералізованный тоніка-клонические эпілептычныя прыступы і лёгачная інфекцыя. Паўторная МРТ прадэманстравала больш тоўстыя і распаўсюджаныя пашкоджанні з ацёкам (мал. 1F), а таксама з’яўленне новага агменю, які назапашвае гадаліній, у левай лобнай долі (мал. 1G).
Абмеркаванне
НКМ — гэта неспадчынны нейрокожный сіндром, які характарызуецца буйнымі або множнымі прыроджанымі скурнымі невусамі і першаснымі меланоцитарными пухлінамі ЦНС, упершыню выяўлены спадаром Ракінтанскім ў 1861 годзе. Паведамляецца, што рызыка НКМ складае 23% у пацыентаў з наяўнасцю на скуры буйных заднесярэдзінных ВМН або множных сатэлітных невусы. Лічыцца, што патагенез НКМ абумоўлены анамальнай праліферацыі папярэднікаў меланоцитов з нервовага грэбня, выкліканай саматычнымі міссенс-мутацыямі, якія ўплываюць на шлях MAPK, асабліва мутацыямі ў генах BRAF і NRAS.
Неўралагічныя сімптомы часцей за ўсё ўзнікаюць у дзяцей, рэдка ў дарослых (у перыяд з 1990 па 2023 гады зарэгістравана ўсяго каля 37 выпадкаў НКМ з клінічным дэбютам ва дарослым узросце). Прыкладна 54% пацыентаў з сімптаматычнай НКМ паміраюць на працягу 3 гадоў пасля з’яўлення сімптомаў, нават не маючы злаякасных новаўтварэнняў, тады як пацыенты з бессімптомнай НКМ маюць звычайную працягласць жыцця. Даследаванні паказалі, што запаленне, звязанае з COVID-19, можа ствараць мікраасяроддзе, якая падтрымлівае праліферацыі опухолевых клетак і ўзнікненне генетычных мутацый, а таксама запускае абуджэнне спячых опухолевых клетак. Акрамя таго, было паказана, што SARS-CoV-2 душыць гены-онкосупрессоры, спрыяючы анкагенезу. У нашай пацыенткі неўралагічныя сімптомы з’явіліся праз 1 месяц пасля заражэння COVID-19 і выкліканага SARS-CoV-2 пашкоджанні гематоэнцефаліческій бар’ера- нейровоспаление магло спрыяць развіццю НКМ, аднак дадзеная здагадка аб прычынна-следчай сувязі патрабуе далей Асноўнымі неўралагічнымі сімптомамі НКМ з’яўляюцца гідрацэфалія, сімптомы, звязаныя з ўнутрычарапной гіпертэнзіяй, а таксама эпілептычныя прыступы. Паражэнне спіннога мозгу сустракаецца прыкладна ў 20% пацыентаў. Пры гэтым хуткапрагрэсавальная дэменцыя і нармальны нутрачарапны ціск, назіраныя ў нашай пацыенткі, не з’яўляюцца тыповымі праявамі НКМ. Вынікі аналізу спіннамазгавой вадкасці пры НКМ звычайна ўключаюць у сябе стэрыльны лейкацытоз, высокі ўзровень бялку, падвышаны пачатковы ціск і нізкі ўзровень глюкозы, што было пацверджана ў рэтраспектыўным даследаванні 13 дарослых пацыентаў з НКС. Аднак вельмі выяўленая гипогликорахия, назіраная ў нашай пацыенткі, пры НКМ сустракаецца вельмі рэдка.
Характэрнымі дадзенымі на МРТ з’яўляюцца дыфузнае лептаменінгеальнае патаўшчэнне ў галаўным і спінным мозгу і дыфузнае лінейнае кантраснае ўзмацненне на T1-ВІ. Пры ўцягванні парэнхімы галаўнога мозгу звычайна візуалізуюцца агмені анамальнага сігналу, асабліва ў міндалепадобным целе, таламуса і лобных долях. МРТ галаўнога мозгу нашай пацыенткі мела ўнікальныя асаблівасці. На МРТ быў бачны незвычайны дыфузны кортикальный меланоз ў абодвух паўшар’ях галаўнога мозгу, што адрознівалася ад тыповай візуалізацыйнай карціны НКМ. Меланоцитома звычайна дае высокую інтэнсіўнасць сігналу на T1-ВІ і нізкую інтэнсіўнасць сігналу T2-ВІ з прычыны парамагнітных уласцівасцяў меланіну, у той час як у нашай пацыенткі ва ўчастках паразы назіраліся высокая інтэнсіўнасць у рэжыме T2 FLAIR і сігнал злёгку падвышаны паказвае на магчымую малігнізацыю з некрозам ці ўжо нізкае ўтрыманне меланіну.
У цяперашні час не існуе адзіных рэкамендацый па лячэнні НКМ, а варыянты лячэння ўключаюць хірургічнае ўмяшанне, хіміятэрапію, прамянёвую тэрапію, імунатэрапію і сімптаматычнае лячэнне. Нягледзячы на нядаўнія дасягненні ў лячэнні злаякаснай меланомы з дапамогай імунатэрапіі кантрольных кропак і таргетнай тэрапіі, накіраванай на BRAF і MEK, прагноз НКМ застаецца незразумелым.
Дадзены рэдкі клінічны выпадак падкрэслівае, што НКМ можа выяўляцца хутка прагрэсавальнай дэменцыяй, а не тыповымі сімптомамі, такімі як нутрачарапная гіпертэнзія, што мае значную клінічную каштоўнасць пры дыферэнцыяльнай дыягностыцы вострай прагрэсавальнай

